Kemokinler
Tümör mikroçevresine NK hücrelerinin spesifik olarak çekilmesi ve aktivasyonu. CXCR3, CX3CR1 reseptörleri ile hedefe yönlendirme.
Hücre Göçü
Önceden eğitime ihtiyaç duymadan, hedefleri anında tanıyan ve yok eden doğal immün sistemin elit savaşçıları.
Etki Mekanizmasını Keşfet ↓Doğal Katil (Natural Killer) hücreler, doğuştan gelen bağışıklık sisteminin en güçlü efektör hücreleridir. Virüsle enfekte olmuş ve tümör hücrelerini önceden bir uyarıya ihtiyaç duymadan tanır ve yok eder.
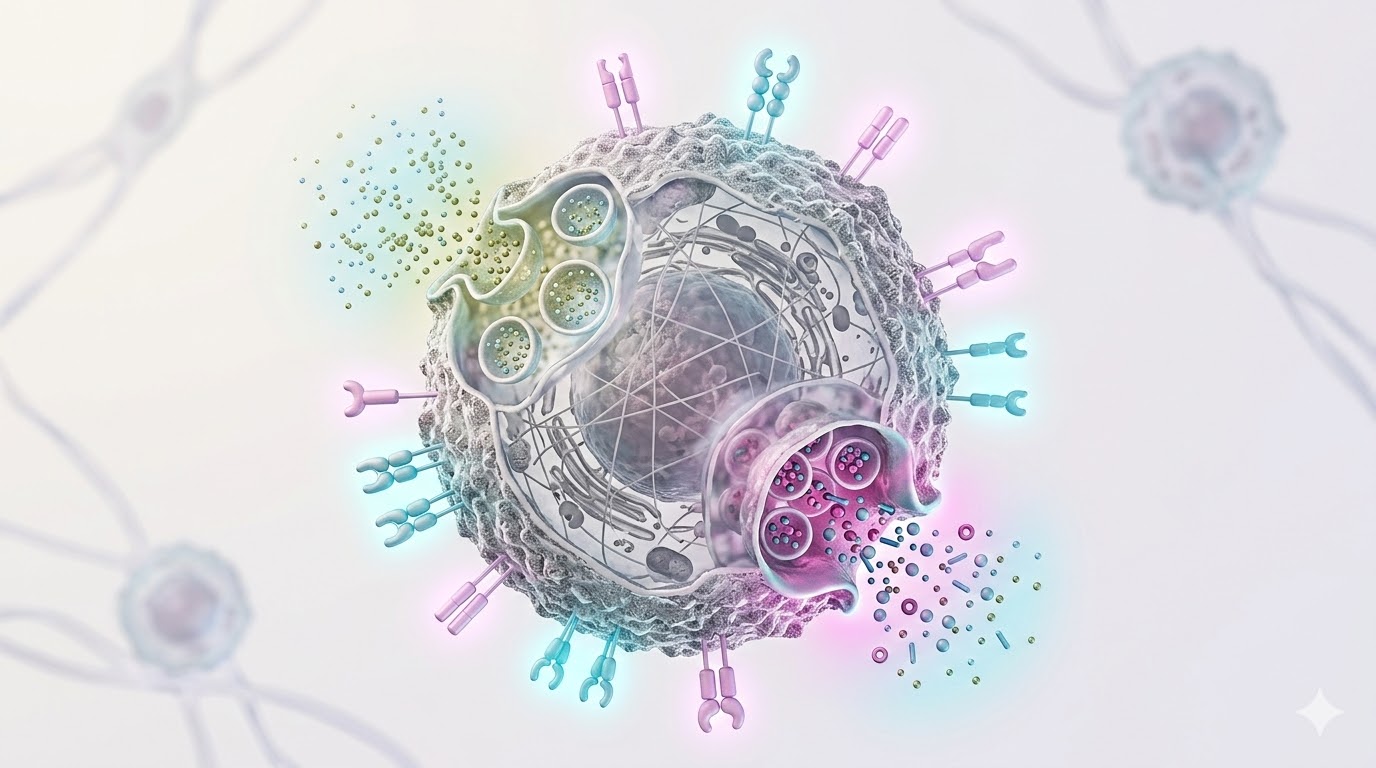
NK hücresinin farklı bölgelerini incelemek için soldaki numaralı noktalara tıklayın.
NKG2D, NKp30, NKp44, NKp46
Stres altındaki, enfekte olmuş veya kanserli hücrelerin yüzeyindeki ligandları tanıyan moleküler sensörler. Bu reseptörler aktive olduğunda NK hücresi "öldür" sinyali alır.
KIR, NKG2A/CD94
Sağlıklı hücrelerin yüzeyindeki MHC sınıf I moleküllerini tanır ve NK hücresine "öldürme" sinyali gönderir. Bu denge sayesinde sağlıklı hücreler korunur. Buna "kendinden olanı tanı" prensibi denir.
Perforin & Granzim B
NK hücresinin silah deposu. Perforin hedef hücre zarında delikler açarken, Granzim B bu deliklerden girerek hücrede programlı ölümü (apoptoz) tetikler. Seri katil gibi birden fazla hedefi arka arkaya yok edebilir.
IFN-γ, TNF-α, GM-CSF
NK hücreleri sadece öldürmez; bağışıklık sisteminin diğer üyelerini de harekete geçiren kimyasal haberciler (sitokinler) salgılar. IFN-γ özellikle makrofajları aktive ederek savunmayı güçlendirir.
Çift katlı lipid membran
NK hücresini çevreleyen akışkan lipid zarı, yüzeyindeki yüzlerce reseptör ve koreseptörü taşır. Zarın akışkanlığı, hücrenin hedefine tutunması (immunolojik sinaps oluşturması) ve granül salınımı için kritik öneme sahiptir.
NK hücresi hedef hücreyi tespit ettiği andan itibaren başlayan 3 aşamalı hassas yıkım süreci. Her adım, bir öncekinin devamıdır.
Hedef Hücreye Kilitlenme
NK hücresi, hedef hücrenin yüzeyindeki stres ligandlarını aktivasyon reseptörleri (NKG2D, NKp30) aracılığıyla tanır. İki hücre arasında "immünolojik sinaps" adı verilen özel bir temas bölgesi oluşur. Bu bölge, aktin filamentlerinin yeniden düzenlenmesiyle sıkı bir yapışma halkası oluşturur. Hedef artık kaçamaz.
Zırh Delici Saldırı
Sinaps oluştuğunda NK hücresi, litik granüllerini sinaps bölgesine yönlendirir. Granüller içindeki perforin molekülleri hedef hücrenin zarına yerleşerek nanometre çapında porlar (delikler) açar. Bu porlar, granzim enzimlerinin hücre içine girmesini sağlayan geçit görevi görür.
Programlı Hücre Ölümü
Perforin porlarından giren Granzim B enzimleri, hedef hücrede kaspaz kaskadını tetikleyerek apoptozu (programlı hücre ölümü) başlatır. DNA fragmantasyonu ve hücre büzülmesi gerçekleşir. NK hücresi hasarsız ayrılır ve seri katil gibi bir sonraki hedefe yönelir.
Dünya genelindeki klinik çalışmalardan derlenen veriler, NK hücrelerinin immünoterapideki gücünü ortaya koymaktadır.
İleri evre lenfoma ve lösemi tanısı almış 11 hastaya, gen mühendisliğiyle güçlendirilmiş NK hücreleri (CAR-NK) uygulandı. Bu hücrelerin görevi şuydu: kanser hücresinin yüzeyindeki CD19 proteinini bulup yok etmek.
• 11 hastanın 8'inde (%73) tümör küçüldü
• 11 hastanın 7'sinde (%64) hastalık tamamen geriledi
Sonuç: Klasik CAR-T tedavisinde sık karşılaşılan üç ciddi yan etki var: aşırı immün yanıtla gelen sitokin fırtınası, nörolojik şikâyetler ve doku reddi. Bu çalışmada hiçbir hastada bunlardan birine rastlanmadı. Yani hem etkili hem güvenli.
Liu et al., N Engl J Med, 2020; 382:545-553NK hücreli kanser tedavisi şu anda dünyanın dört bir yanında insanlar üzerinde deneniyor. ABD'nin tüm tıbbi araştırma kayıtlarını tuttuğu ClinicalTrials.gov verilerine göre tablo şöyle:
• 2021 sonunda 420 NK çalışması kayıtlıydı
• 2016'dan bu yana her yıl ortalama 47 yeni çalışma başlıyor
• Bugün gelinen rakam 500'ün üzerinde
Sonuç: Onkolojide en hızlı büyüyen araştırma alanlarından biri NK hücre tedavisi. Yıllık iki haneli artış, alanın hem akademik hem ticari ağırlığını gösteriyor.
Heipertz et al., J Hematol Oncol, 2022; 15:184 · PubMedNK hücre tedavisi 20'den fazla farklı kanser türünde araştırılıyor:
• Kan kanserleri: akut ve kronik lösemiler (AML, ALL), lenfoma (NHL), multipl miyelom
• Katı tümörler: akciğer, yumurtalık, pankreas, beyin (glioblastom), melanom, kalın bağırsak, meme
Gen mühendisliğiyle güçlendirilmiş NK (CAR-NK) çalışmalarının dağılımına bakınca da şu görülüyor: %54 kan kanseri, %34 katı tümör, %11 otoimmün hastalık.
Sonuç: Çoğu kanser hücresi, immün sistemden saklanmak için yüzeyindeki MHC moleküllerini gizler. NK hücrelerinin avantajı işte burada: bu numaraya takılmazlar. Bu sayede geniş bir tümör yelpazesine, hatta diğer immün hücrelerin ulaşamadığı kanserlere bile erişebiliyor.
Gong et al., Exp Hematol Oncol, 2024; 13:18Yüksek çözünürlüklü mikroskoplarla yapılan tek hücre görüntüleme çalışmalarında, NK hücresinin tümöre değdiği andan itibaren ne olduğu adım adım takip edildi:
• Temastan sonraki ilk birkaç dakika içinde NK hücresi delici protein (perforin) ve enzim (granzim B) salgılıyor
• Tümör hücresi 10-15 dakikada ölüm sürecine giriyor
• Aynı NK hücresi ardından başka bir hedefe yöneliyor
Sonuç: Tek bir NK hücresi arka arkaya 20'den fazla tümör hücresini yok edebilir. Hem hızlı hem ekonomik bir savunma. Birçok immün hücrenin aksine, NK "tek atımlık" değil.
Prager et al., J Exp Med, 2019; 216(9):2113-2127 · PubMedDetaylar için kartlara tıklayın
NK hücre tedavisi, hücresel immünoterapiler arasında en düşük yan etki profillerinden birine sahiptir. Klinik çalışmalarda kanıtlanmış güvenlik verileri.
Klinik çalışmalarda NK hücre tedavisi alan hastalarda sitokin salınım sendromu (CRS) gözlenmemiştir. Kontrollü immün yanıt oluşturur.
Merkezi sinir sistemi üzerinde olumsuz etki raporlanmamıştır. NK hücreleri hedef dışı doku hasarı oluşturmaz.
NK hücreleri T hücre reseptörü (TCR) taşımadığı için sağlıklı dokuları hedef alamaz. Klinik çalışmalarda allojenik (donör kaynaklı) NK kullanımında GvHD vakası bildirilmedi.
Önceden hazırlanmış "off-the-shelf" tedavi imkanı. Kişiye özel üretim gerektirmez, tedaviye hızlı başlangıç sağlar.
MHC-bağımsız çalışarak antijen kaçış mekanizmalarına karşı dirençlidir. Birden fazla yolakla hedefi tanır ve yok eder.
Tek bir NK hücresi hasarsız ayrılarak arka arkaya ~20 hedef hücreyi yok edebilir. Tedavi boyunca aktif kalır.
Liu et al., NEJM 2020 • Heipertz et al., J Hematol Oncol 2022
Doğal katil hücrelerin kanserle savaşma potansiyelini artırmak için laboratuvar ortamında geliştirilen 6 temel yaklaşım.
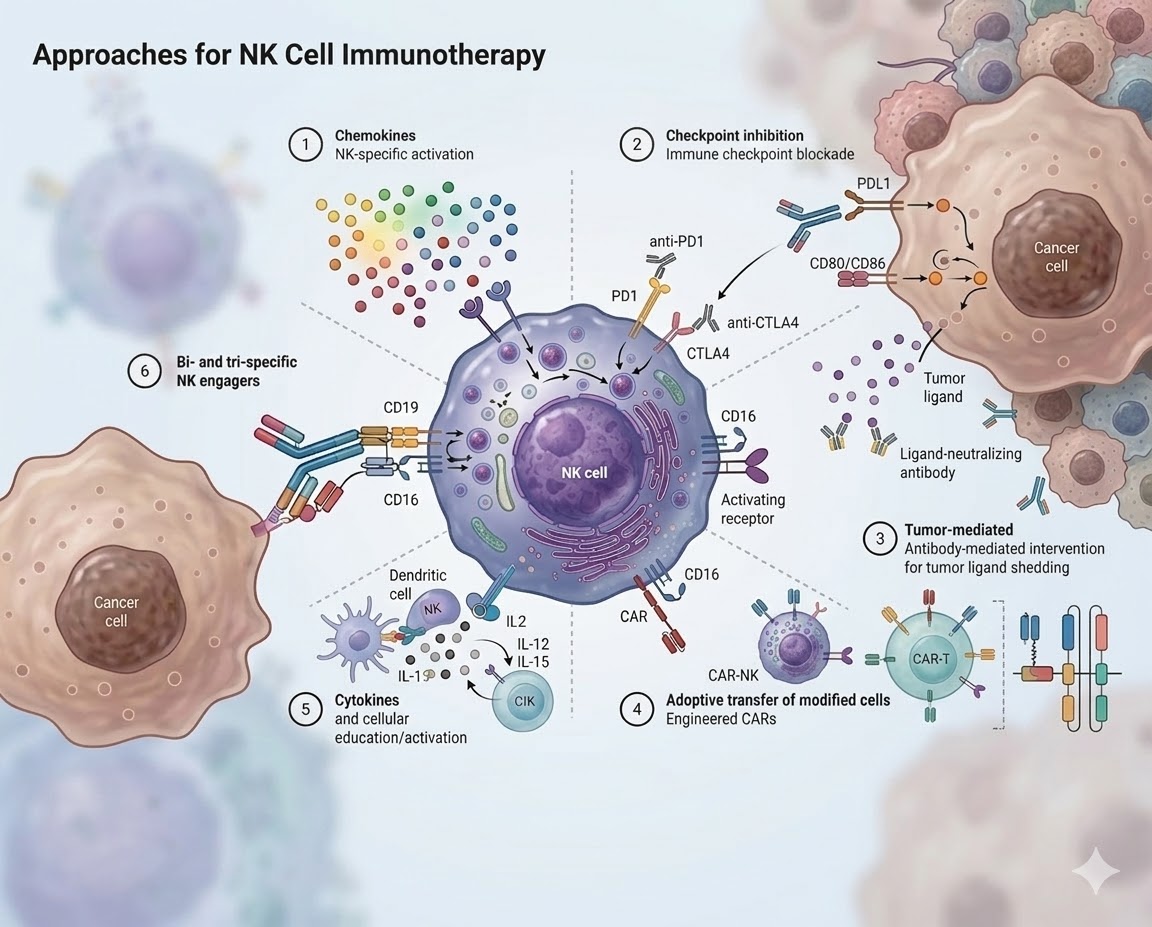

Tümör mikroçevresine NK hücrelerinin spesifik olarak çekilmesi ve aktivasyonu. CXCR3, CX3CR1 reseptörleri ile hedefe yönlendirme.
Hücre Göçü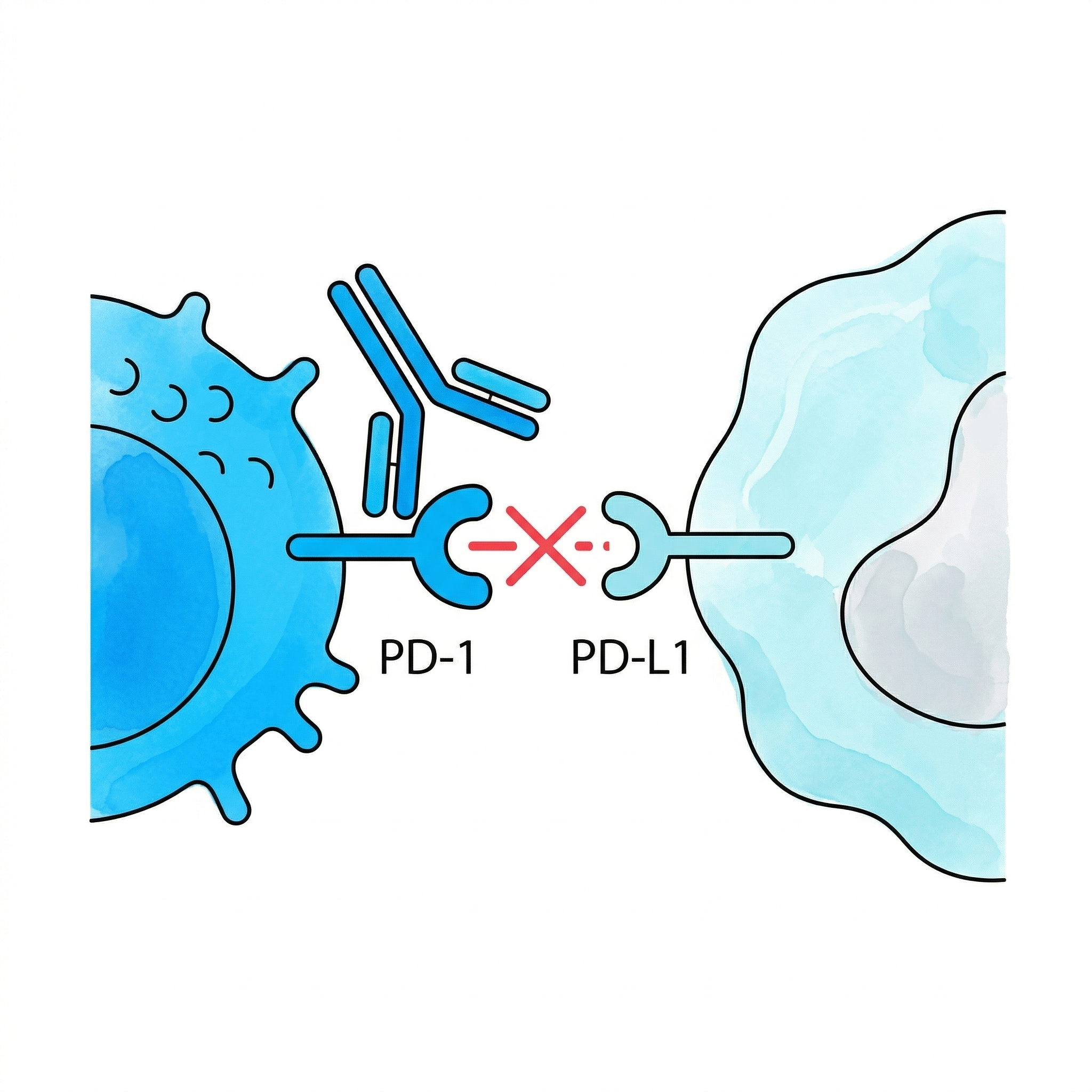
PD-1, CTLA-4 gibi "fren" reseptörlerinin bloke edilmesi. Anti-PD1 ve anti-CTLA4 antikorları NK aktivitesini serbest bırakır.
İmmün Kaçış Engeli
Tümör ligandlarının dökülmesini engelleyen antikor aracılı müdahaleler. Ligand-nötralize edici antikorlar kaçış mekanizmasını devre dışı bırakır.
Ligand Blokajı
CAR-NK ve CAR-T gibi genetik olarak modifiye edilmiş hücrelerin hastaya aktarımı. Kimerik antijen reseptörleri (CAR) ile hedef-spesifik donatım.
Hücre Mühendisliği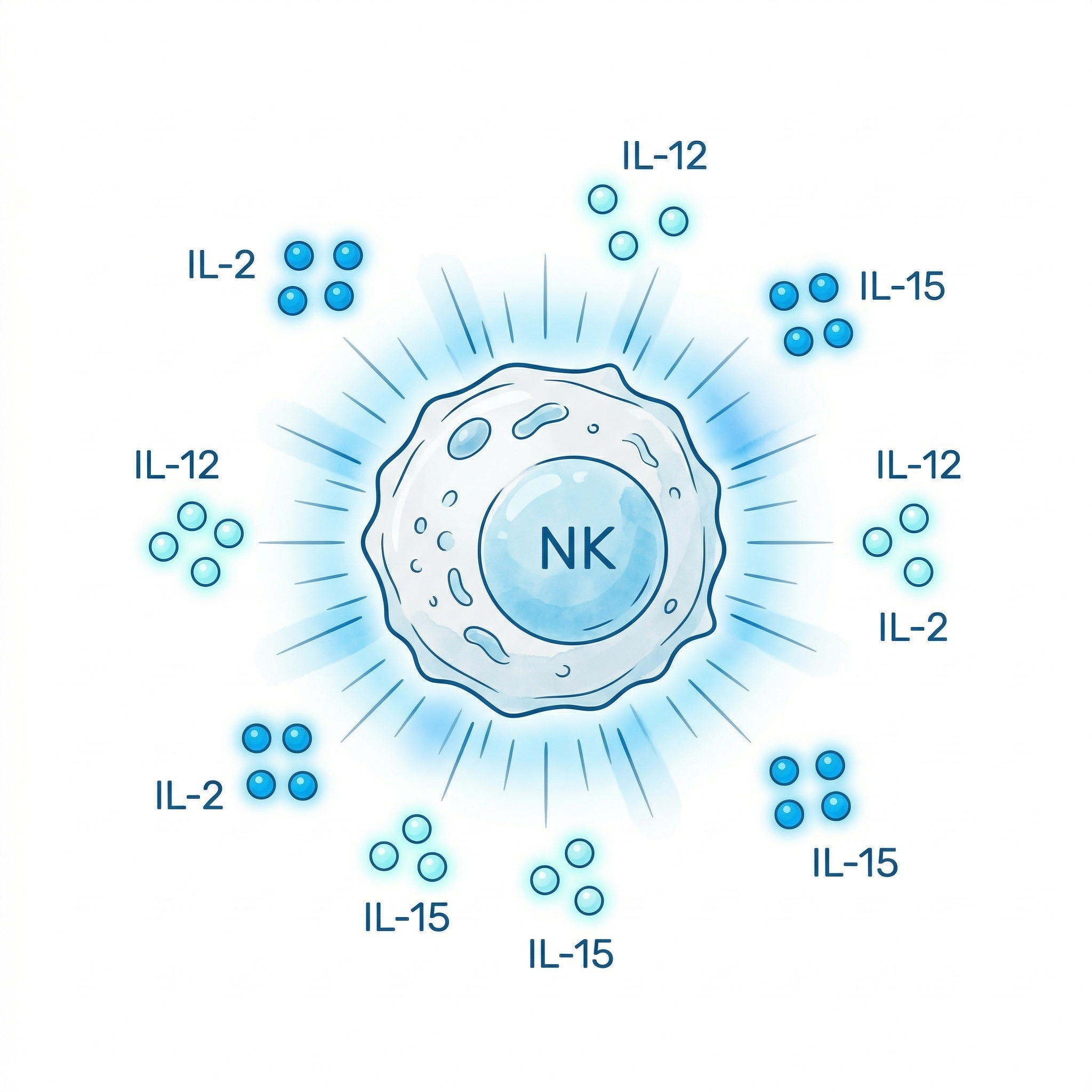
IL-2, IL-12, IL-15 ile hücresel eğitim, çoğalma ve aktivasyon. CIK (Sitokin İndüklü Katil) hücreler bu yöntemle ex vivo üretilir.
Sitokin Terapisi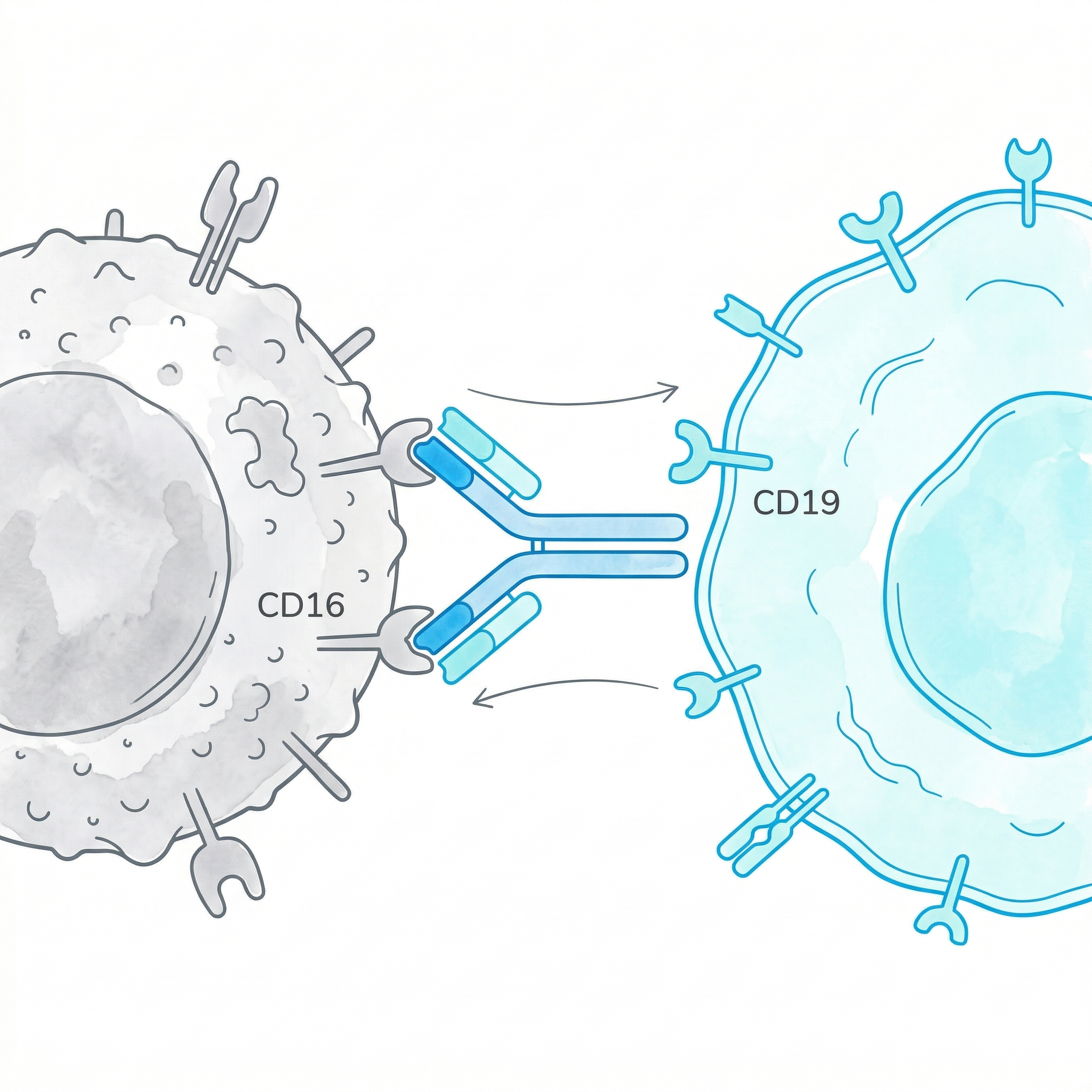
NK hücresini doğrudan kanser hücresine bağlayan özel köprü moleküller. CD16 ve CD19 üzerinden eş zamanlı yakalama.
Hedefli BağlanmaNK hücrelerini kendi AR-GE laboratuvarımızda, uluslararası standartlarda geliştiriyor ve üretiyoruz. Yerli üretim, global kalite.

NK hücrelerini dış kaynaklara bağımlı olmadan, kendi GMP uyumlu AR-GE tesislerimizde geliştiriyor ve üretiyoruz.
Hücre izolasyonundan ekspansiyona, kalite kontrolden klinik uygulamaya kadar tüm süreçleri tek çatı altında yönetiyoruz.
GMP (İyi Üretim Uygulamaları) standartlarına uygun süreçler, uluslararası sertifikasyonlar ve sürekli denetim altyapısı.
NK hücresi, CIK ve Dendritik Hücre dahil bakanlık onaylı immünoterapi ürünlerini kendi laboratuvarımızda üretmekteyiz.
NK hücreleri, CAR-T gibi diğer hücresel tedavilere kıyasla önemli ölçüde daha güvenli bir profile sahiptir. CAR-T tedavisinde sıkça görülen sitokin salınım sendromu (CRS) ve nörotoksisite riskleri, NK hücre tedavisinde son derece düşüktür. Bunun nedeni, NK hücrelerinin doğal bağışıklık sisteminin bir parçası olarak daha kontrollü bir immün yanıt oluşturmasıdır.
NK hücreleri bugüne kadar 20'den fazla farklı kanser türünde araştırıldı. En yüksek yanıt oranları kan kanserlerinde (lösemi, lenfoma) görüldü. Solid (katı) tümörlerde de umut verici sonuçlar var: akciğer, yumurtalık ve kalın bağırsak kanseri başta gelenler.
CAR-T tedavisi hastanın kendi T hücrelerini genetik olarak değiştirmeyi gerektirir; bu kişiye özel, maliyetli ve uzun süren bir süreçtir. NK hücreleri ise donörden (allojenik) alınarak kullanılabilir. Yani önceden hazırlanmış, "raf ürünü" tedavi mümkündür. Bu hem maliyeti düşürür, hem erişimi artırır, hem de tedaviye başlama süresini kısaltır.
Genkord, 2003'ten bu yana hücre biyolojisi alanında çalışıyor. NK hücrelerini kendi cGMP sertifikalı laboratuvarında, hücre izolasyonundan çoğaltmaya kadar tüm aşamaları kendi kontrolü altında üretmeyi planlıyor. Şu an 15'ten fazla biyolojik ürün (mezenkimal kök hücre ve eksozom serileri) üretiyor.
NK hücre tedavileri dünya genelinde 500'den fazla klinik çalışmada aktif olarak araştırılıyor. Bazı NK bazlı tedaviler artık Faz 2 ve Faz 3 aşamalarına ulaştı. Genkord olarak bu alandaki gelişmeleri yakından takip ediyor, kendi üretim altyapımızı da bu hedefe göre hazırlıyoruz.
NK hücreleri T hücre reseptörü (TCR) taşımadığı için sağlıklı dokuları tanıyıp saldırma kapasitesi yoktur. Allojenik NK transfer çalışmalarında (Miller ve ark., Blood 2005; Liu ve ark., NEJM 2020) GvHD vakası bildirilmedi. Bu nedenle farklı donörlerden alınan NK hücreleri klinik açıdan güvenli kabul ediliyor; yine de her hücresel terapide olduğu gibi resmi güvenlik takibi sürdürülüyor.
NK hücre tedavileri, AR-GE iş birlikleri veya klinik çalışma ortaklıkları hakkında bilgi almak için ekibimizle iletişime geçin.